Gazele, din punct de vedere al termodinamicii, sunt descrise printr-un set de caracteristici macroscopice, dintre care principalele sunt temperatura, presiunea și volumul. Constanța unuia dintre acești parametri și modificarea celorlalți doi indică faptul că în gaz are loc unul sau altul izoproces. Vom dedica acest articol unui răspuns detaliat la întrebările că acesta este un proces izocor, cum diferă de schimbările izoterme și izobare în stările unui sistem de gaze.
Gaz ideal în fizică

Înainte de a răspunde la întrebarea că acesta este un proces izocor, ar trebui să cunoașteți mai bine conceptul de gaz ideal. În fizică, este înțeles ca orice gaz în care energia cinetică medie a particulelor sale constitutive depășește cu mult energia potențială a interacțiunii lor, iar distanțele dintre aceste particule sunt cu câteva ordine de mărime mai mari decât dimensiunile lor liniare. În condițiile menționate, este posibil, în timpul efectuăriicalculele nu iau în considerare energia de interacțiune dintre particule (este egală cu zero) și se poate presupune, de asemenea, că particulele sunt puncte materiale cu o anumită masă m.
Singurul proces care are loc într-un gaz ideal este ciocnirea particulelor cu pereții vasului care conține substanța. Aceste ciocniri se manifestă în practică ca existența unei anumite presiuni în gazul P.
De regulă, orice substanță gazoasă care constă din molecule relativ inerte din punct de vedere chimic și care are presiune scăzută și temperaturi ridicate poate fi considerată un gaz ideal cu suficientă precizie pentru calcule practice.
Ecuație care descrie un gaz ideal
Desigur, vorbim despre legea universală a lui Clapeyron-Mendeleev, care ar trebui bine înțeleasă pentru a înțelege că acesta este un proces izocor. Deci, ecuația universală de stare are următoarea formă:
PV=nRT.
Adică produsul presiunii P și volumul gazului V este egal cu produsul dintre temperatura absolută T și cantitatea de substanță în moli n, unde R este factorul de proporționalitate. Ecuația în sine a fost scrisă pentru prima dată de Emile Clapeyron în 1834, iar în anii 70 ai secolului al XIX-lea, D. Mendeleev a înlocuit în ea un set de valori constante ale unei singure constante universale de gaz R (8,314 J/(molK).)).
În conformitate cu ecuația Clapeyron-Mendeleev, într-un sistem închis numărul de particule de gaz rămâne constant, deci există doar trei parametri macroscopici care se pot modifica (T, Pși V). Acest din urmă fapt stă la baza înțelegerii diferitelor izoprocese care vor fi discutate mai jos.
Ce este un proces izocor?
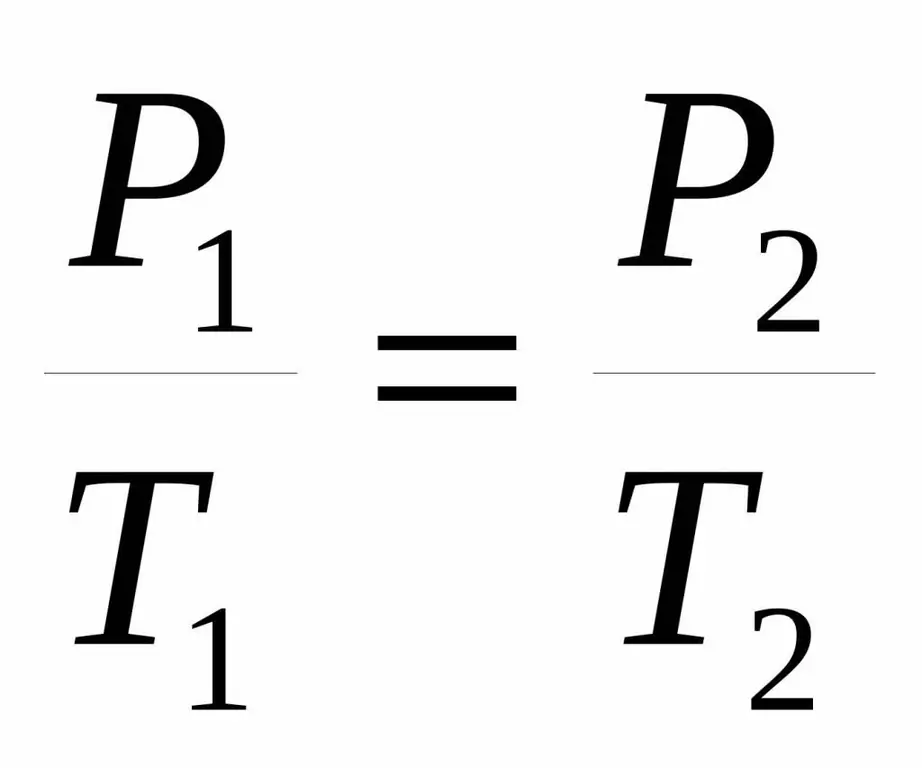
Acest proces este înțeles ca absolut orice modificare a stării sistemului, în care volumul acestuia este păstrat.
Dacă ne întoarcem la ecuația universală de stare, putem spune că într-un proces izocor doar presiunea și temperatura absolută se modifică într-un gaz. Pentru a înțelege exact cum se modifică parametrii termodinamici, scriem expresia matematică corespunzătoare:
P / T=const.
Uneori, această egalitate este dată într-o formă ușor diferită:
P1 / T1=P2 / T 2.
Ambele egalități sunt numite legea lui Charles după numele unui om de știință francez care la sfârșitul secolului al XVIII-lea a obținut în mod experimental dependența remarcată.

Dacă construim un grafic al funcției P(T), atunci obținem o dependență de linie dreaptă, care se numește izocor. Orice izocor (pentru toate valorile lui n și V) este o linie dreaptă.
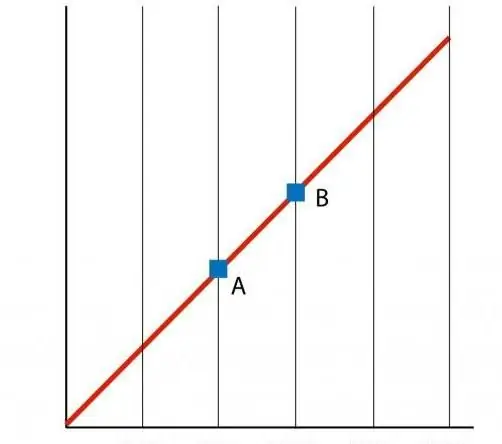
Descrierea energetică a procesului
După cum sa menționat, un proces izocor este o schimbare a stării unui sistem care are loc într-un sistem închis, dar nu izolat. Vorbim despre posibilitatea schimbului de căldură între gaz și mediu. În general, orice furnizare de căldură Q către sistem duce la două rezultate:
- schimbă energia internă U;
- gazfuncționează A, se extinde sau se contractă.
Ultima concluzie este scrisă matematic după cum urmează:
Q=U + A.
Procesul izocor al unui gaz ideal, prin definiția sa, nu implică muncă efectuată de gaz, deoarece volumul acestuia rămâne neschimbat. Aceasta înseamnă că toată căldura furnizată sistemului merge pentru a-i crește energia internă:
Q=U.
Dacă substituim formula explicită pentru energia internă în această expresie, atunci căldura procesului izocor poate fi reprezentată ca:
Q=z / 2nRT.
Aici z este numărul de grade de libertate, care este determinat de natura poliatomică a moleculelor care formează gazul. Pentru un gaz monoatomic, z=3, pentru un gaz diatomic - 5, iar pentru un triatomic și mai mult - 6. Aici, sub grade de libertate, înțelegem grade de translație și rotație.
Dacă comparăm eficiența încălzirii unui sistem de gaz în procesele izocorice și izobare, atunci în primul caz vom obține eficiența maximă, deoarece în timpul schimbării izobare a stării sistemului, gazul se dilată și o parte din consumul de căldură este cheltuit pentru a lucra.
Proces izobaric
Mai sus am descris în detaliu că acesta este un proces izocor. Acum să spunem câteva cuvinte despre alte izoprocese. Să începem cu izobaric. Pe baza numelui, se înțelege ca trecerea sistemului între stări la presiune constantă. Acest proces este descris de legea Gay-Lussac după cum urmează:
V / T=const.
Ca și în cazul izocorului, izobara V(T) reprezintă, de asemenea, o linie dreaptă pe grafic.
Pentrua oricărui proces izobaric, este convenabil să se calculeze munca efectuată de gaz, deoarece este egal cu produsul presiunii constante și modificarea volumului.
Proces izotermic
Acesta este un proces în care temperatura sistemului rămâne constantă. Este descris de legea Boyle-Mariotte pentru un gaz ideal. Este curios de observat că aceasta este prima lege a gazelor descoperită experimental (a doua jumătate a secolului al XVII-lea). Notația sa matematică arată astfel:
PV=const.
Procesele izocorice și izoterme diferă în ceea ce privește reprezentarea lor grafică, deoarece funcția P(V) este o relație hiperbolică, nu liniară.
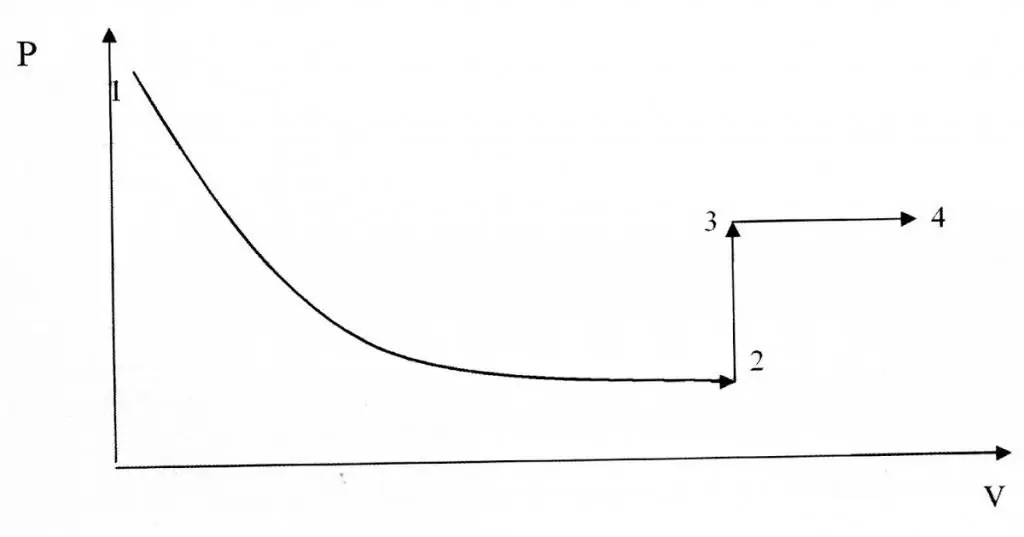
Exemplu de rezolvare a problemelor
Să consolidăm informațiile teoretice furnizate în articol de aplicarea lor pentru a rezolva o problemă practică. Se știe că azotul gazos pur se afla într-un cilindru la o presiune de 1 atmosferă și o temperatură de 25 °C. După ce cilindrul de gaz a fost încălzit și a fost măsurată presiunea din ea, sa dovedit a fi de 1,5 atmosfere. Care este temperatura gazului din butelie după încălzire? Cu ce cantitate s-a schimbat energia internă a gazului dacă erau 4 moli de azot în balon.
Pentru a răspunde la prima întrebare, folosim următoarea expresie:
P1 / T1=P2 / T 2.
De unde obținem:
T2=P2 / P1 T 1.
În această expresie, presiunea poate fi înlocuită în unități arbitraremăsurători, deoarece se micșorează, iar temperatura este doar în kelvins. Acestea fiind spuse, obținem:
T2=1,5 /1298,15=447,224 K.
Temperatura calculată în grade Celsius este de 174 °C.
Deoarece molecula de azot este diatomică, modificarea energiei sale interne în timpul încălzirii poate fi determinată după cum urmează:
ΔU=5 / 2nRΔT.
Înlocuind valorile cunoscute în această expresie, vom obține răspunsul la a doua întrebare a problemei: ΔU=+12,4 kJ.






