În termodinamică, atunci când se studiază tranzițiile de la starea inițială la cea finală a unui sistem, este important să se cunoască efectul termic al procesului. Conceptul de capacitate termică este strâns legat de acest efect. În acest articol, vom lua în considerare întrebarea ce se înțelege prin capacitatea termică izocoră a unui gaz.
Gaz ideal
Un gaz ideal este un gaz ale cărui particule sunt considerate puncte materiale, adică nu au dimensiuni, ci au masă și în care toată energia internă constă numai din energia cinetică a mișcării moleculelor. și atomi.
Orice gaz real în mod ideal nu va satisface niciodată modelul descris, deoarece particulele sale au încă niște dimensiuni liniare și interacționează între ele folosind legături slabe van der Waals sau legături chimice de alt tip. Cu toate acestea, la presiuni scăzute și la temperaturi ridicate, distanțele dintre molecule sunt mari, iar energia lor cinetică depășește de zeci de ori energia potențială. Toate acestea fac posibilă aplicarea cu un grad ridicat de acuratețe a modelului ideal pentru gaze reale.
Energia internă a gazului
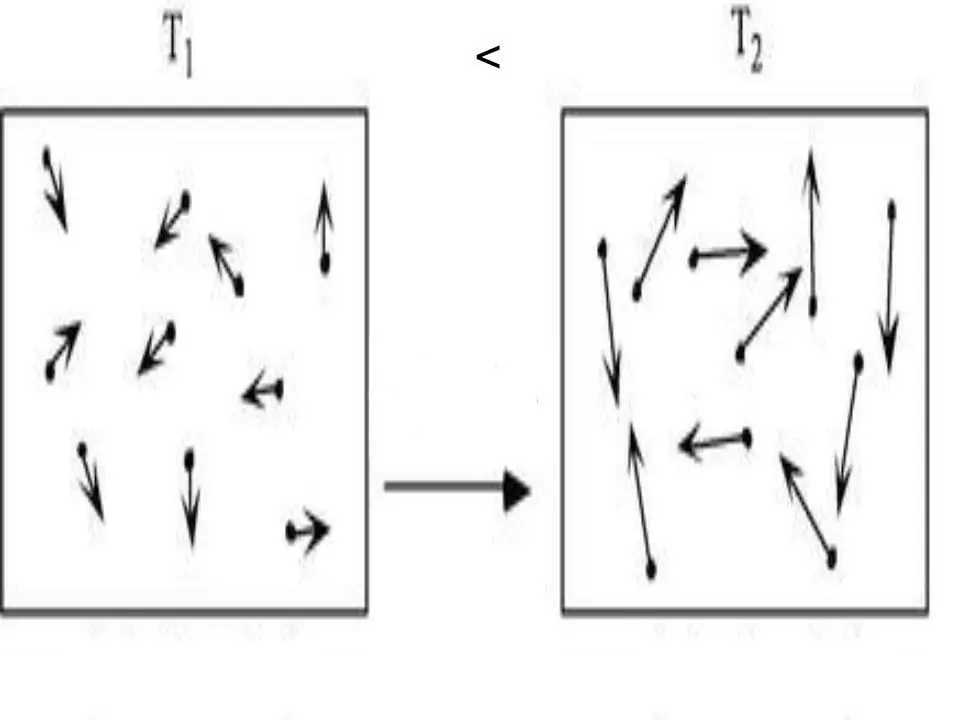
Energia internă a oricărui sistem este o caracteristică fizică, care este egală cu suma energiei potențiale și cinetice. Deoarece energia potențială poate fi neglijată în gazele ideale, putem scrie egalitatea pentru ele:
U=Ek.
Unde Ek este energia sistemului cinetic. Folosind teoria cinetică moleculară și aplicând ecuația de stare universală Clapeyron-Mendeleev, nu este greu de obținut o expresie pentru U. Se scrie mai jos:
U=z/2nRT.
Aici T, R și n sunt temperatura absolută, constanta gazului și respectiv cantitatea de substanță. Valoarea z este un număr întreg care indică numărul de grade de libertate pe care le are o moleculă de gaz.
Capacitate termică izobară și izocoră
În fizică, capacitatea de căldură este cantitatea de căldură care trebuie furnizată sistemului studiat pentru a-l încălzi cu un kelvin. Definiția inversă este, de asemenea, adevărată, adică capacitatea de căldură este cantitatea de căldură pe care sistemul o eliberează atunci când este răcit cu un kelvin.
Cea mai simplă modalitate pentru un sistem este de a determina capacitatea termică izocoră. Se înțelege ca fiind capacitatea termică la volum constant. Deoarece sistemul nu efectuează lucrări în astfel de condiții, toată energia este cheltuită pentru creșterea rezervelor interne de energie. Să notăm capacitatea termică izocoră prin simbolul CV, apoi putem scrie:
dU=CVdT.
Adică schimbarea energiei internesistemul este direct proporțional cu modificarea temperaturii sale. Dacă comparăm această expresie cu egalitatea scrisă în paragraful anterior, ajungem la formula pentru CV într-un gaz ideal:
СV=z/2nR.
Această valoare este incomod de utilizat în practică, deoarece depinde de cantitatea de substanță din sistem. Prin urmare, a fost introdus conceptul de capacitate termică specifică izocoră, adică o valoare care se calculează fie la 1 mol de gaz, fie la 1 kg. Să notăm prima valoare prin simbolul CV, a doua - prin simbolul CV m. Pentru ei, puteți scrie următoarele formule:
CV=z/2R;
CVm=z/2R/M.
Aici M este masa molară.
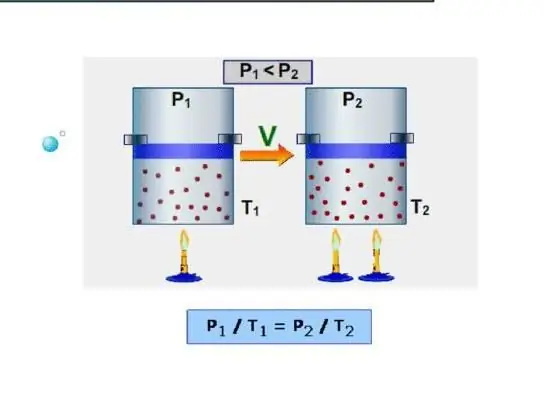
Isobaric este capacitatea de căldură menținând în același timp o presiune constantă în sistem. Un exemplu de astfel de proces este expansiunea gazului într-un cilindru sub un piston atunci când este încălzit. Spre deosebire de procesul izocor, în timpul procesului izobar, căldura furnizată sistemului este cheltuită pentru a crește energia internă și pentru a efectua lucrări mecanice, adică:
H=dU + PdV.
Entalpia unui proces izobar este produsul dintre capacitatea termică izobară și modificarea temperaturii în sistem, adică:
H=CPdT.
Dacă luăm în considerare dilatarea la o presiune constantă de 1 mol de gaz, atunci prima lege a termodinamicii se va scrie ca:
CPdT=CV dT + RdT.
Ultimul termen se obține din ecuațieClapeyron-Mendeleev. Din această egalitate rezultă relația dintre capacitățile termice izobare și izocorice:
CP=CV + R.
Pentru un gaz ideal, capacitatea de căldură molară specifică la presiune constantă este întotdeauna mai mare decât caracteristica izochoră corespunzătoare cu R=8, 314 J/(molK).
Grade de libertate a moleculelor și capacitatea termică
Să scriem din nou formula pentru capacitatea termică izocoră molară specifică:
CV=z/2R.
În cazul unui gaz monoatomic, valoarea z=3, deoarece atomii din spațiu se pot mișca doar în trei direcții independente.
Dacă vorbim despre un gaz format din molecule diatomice, de exemplu, oxigen O2 sau hidrogen H2, atunci, pe lângă mișcarea de translație, aceste molecule se pot roti în continuare în jurul a două axe reciproc perpendiculare, adică z va fi egal cu 5.
Pentru molecule mai complexe, utilizați z=6. pentru a determina CV






