Gazul ideal, ecuația de stare a gazului ideal, temperatura și presiunea acestuia, volumul… lista de parametri și definiții utilizate în secțiunea corespunzătoare de fizică poate fi continuată destul de mult timp. Astăzi vom vorbi doar despre acest subiect.
Ce este considerat în fizica moleculară?

Obiectul principal luat în considerare în această secțiune este un gaz ideal. Ecuația de stare a gazului ideal a fost obținută ținând cont de condițiile normale de mediu și despre asta vom vorbi puțin mai târziu. Acum să abordăm această „problema” de departe.
Să presupunem că avem o masă de gaz. Starea sa poate fi determinată folosind trei parametri de natură termodinamică. Acestea sunt, desigur, presiunea, volumul și temperatura. Ecuația stării sistemului în acest caz va fi formula pentru relația dintre parametrii corespunzători. Arată astfel: F (p, V, T)=0.
Aici, pentru prima dată, ne apropiem încet de apariția unui astfel de lucru ca idealgaz. Se numește gaz în care interacțiunile dintre molecule sunt neglijabile. În general, acest lucru nu există în natură. Cu toate acestea, orice gaz extrem de rarefiat este aproape de el. Azotul, oxigenul și aerul, care se află în condiții normale, diferă puțin de ideal. Pentru a scrie ecuația de stare pentru un gaz ideal, putem folosi legea unificată a gazelor. Se obține: pV/T=const.
Concept corelat 1: Legea lui Avogadro
El ne poate spune că dacă luăm același număr de moli de absolut orice gaz aleatoriu și îi punem în aceleași condiții, inclusiv temperatură și presiune, atunci gazele vor ocupa același volum. În special, experimentul a fost efectuat în condiții normale. Aceasta înseamnă că temperatura a fost de 273,15 Kelvin, presiunea a fost de o atmosferă (760 milimetri de mercur, sau 101325 Pascali). Cu acești parametri, gazul a ocupat un volum egal cu 22,4 litri. Prin urmare, putem spune că pentru un mol de orice gaz, raportul parametrilor numerici va fi o valoare constantă. De aceea s-a decis să desemnăm această cifră cu litera R și să o numim constanta universală a gazelor. Astfel, este egal cu 8,31. Unitatea este J/molK.
Gaz ideal. Ecuația de stare a gazului ideal și manipularea acesteia
Să încercăm să rescriem formula. Pentru a face acest lucru, îl scriem sub această formă: pV=RT. Apoi, efectuăm o acțiune simplă, înmulțim ambele părți ale ecuației cu un număr arbitrar de moli. Se obține pVu=uRT. Să luăm în considerare faptul că produsul volumului molar șicantitatea de materie este pur și simplu volumul. Dar la urma urmei, numărul de moli va fi simultan egal cu câtul dintre masă și masa molară. Exact așa arată ecuația Mendeleev-Clapeyron. Oferă o idee clară despre ce tip de sistem se formează un gaz ideal. Ecuația de stare pentru un gaz ideal va lua forma: pV=mRT/M.
Deduceți formula pentru presiune
Să facem mai multe manipulări cu expresiile obținute. Pentru a face acest lucru, partea dreaptă a ecuației Mendeleev-Clapeyron este înmulțită și împărțită la numărul Avogadro. Acum ne uităm cu atenție la produsul cantității de substanță prin numărul Avogadro. Acesta nu este altceva decât numărul total de molecule din gaz. Dar, în același timp, raportul dintre constanta universală a gazului și numărul Avogadro va fi egal cu constanta Boltzmann. Prin urmare, formulele pentru presiune pot fi scrise după cum urmează: p=NkT/V sau p=nkT. Aici simbolul n este concentrația de particule.
Procese de gaze ideale
În fizica moleculară există așa ceva ca izoprocesele. Acestea sunt procese termodinamice care au loc în sistem la unul dintre parametrii constanți. În acest caz, masa substanței trebuie să rămână constantă. Să le privim mai precis. Deci, legile unui gaz ideal.
Presiunea rămâne constantă
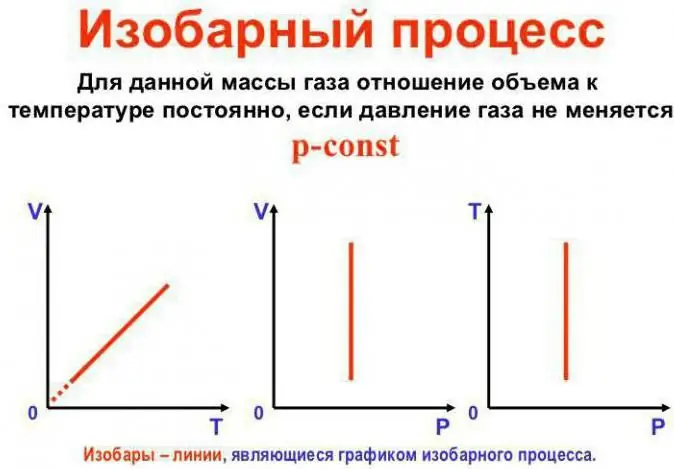
Aceasta este legea lui Gay-Lussac. Arata astfel: V/T=const. Poate fi rescris într-un alt mod: V=Vo (1 + at). Aici a este egal cu 1/273,15 K^-1 și se numește „coeficient de expansiune în volum”. Putem înlocui temperatura atât în Celsius, cât șiscara Kelvin. În ultimul caz, obținem formula V=Voat.
Volumul rămâne constant

Aceasta este a doua lege a lui Gay-Lussac, denumită mai frecvent legea lui Charles. Arata astfel: p/T=const. Există o altă formulare: p=po (1 + at). Transformările pot fi efectuate în conformitate cu exemplul anterior. După cum puteți vedea, legile gazelor ideale sunt uneori destul de asemănătoare între ele.
Temperatura rămâne constantă

Dacă temperatura unui gaz ideal rămâne constantă, atunci putem obține legea Boyle-Mariotte. Poate fi scris astfel: pV=const.
Concept corelat 2: Presiune parțială
Să spunem că avem un vas cu gaze. Va fi un amestec. Sistemul este într-o stare de echilibru termic, iar gazele în sine nu reacţionează între ele. Aici N va desemna numărul total de molecule. N1, N2 și, respectiv, numărul de molecule din fiecare dintre componentele amestecului. Să luăm formula presiunii p=nkT=NkT/V. Poate fi deschis pentru un caz anume. Pentru un amestec cu două componente, formula va lua forma: p=(N1 + N2) kT/V. Dar apoi se dovedește că presiunea totală va fi însumată din presiunile parțiale ale fiecărui amestec. Deci, va arăta ca p1 + p2 și așa mai departe. Acestea vor fi presiunile parțiale.
Pentru ce este?
Formula pe care am obținut-o indică faptul că presiunea din sistem este din fiecare grup de molecule. De altfel, nu depinde dealții. D alton a profitat de acest lucru atunci când a formulat legea, numită ulterior după el: într-un amestec în care gazele nu reacţionează chimic între ele, presiunea totală va fi egală cu suma presiunilor parţiale.






