Când se studiază comportamentul gazelor în fizică, se acordă multă atenție izoproceselor, adică unor astfel de tranziții între stările sistemului, în timpul cărora se păstrează un parametru termodinamic. Cu toate acestea, există o tranziție de gaz între stări, care nu este un izoproces, dar care joacă un rol important în natură și tehnologie. Acesta este un proces adiabatic. În acest articol, îl vom analiza mai detaliat, concentrându-ne asupra exponentului adiabatic al gazului.
Proces adiabatic
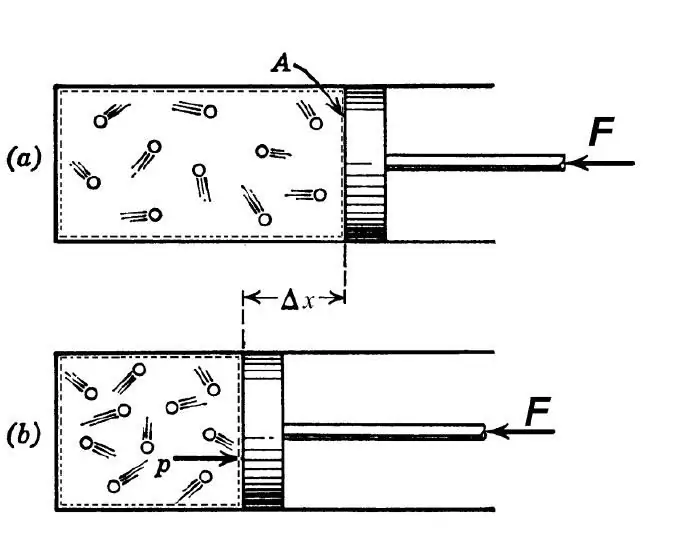
După definiția termodinamică, un proces adiabatic este înțeles ca o astfel de tranziție între stările inițiale și cele finale ale sistemului, în urma căreia nu există schimb de căldură între mediul extern și sistemul studiat. Un astfel de proces este posibil în următoarele două condiții:
- conductivitate termică între mediul extern șisistemul este scăzut dintr-un motiv sau altul;
- viteza procesului este mare, astfel încât schimbul de căldură nu are timp să aibă loc.
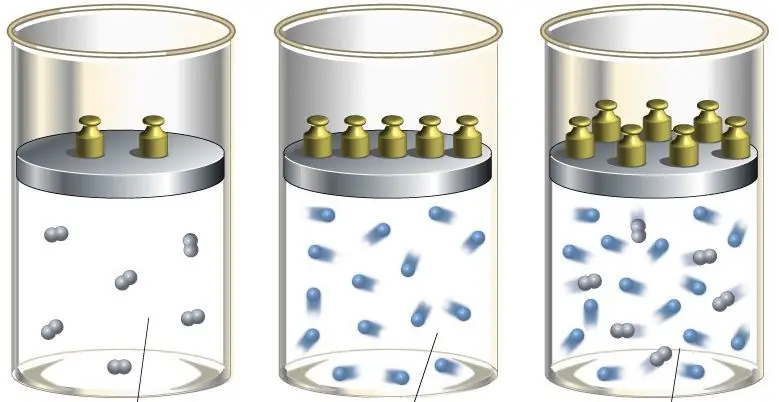
În inginerie, tranziția adiabatică este utilizată atât pentru a încălzi gazul în timpul comprimării sale puternice, cât și pentru a-l răci în timpul expansiunii rapide. În natură, tranziția termodinamică în cauză se manifestă atunci când o masă de aer se ridică sau coboară pe versantul unui deal. Astfel de urcușuri și coborâșuri duc la modificarea punctului de rouă în aer și la precipitații.
Ecuația lui Poisson pentru gazul ideal adiabatic

Un gaz ideal este un sistem în care particulele se mișcă aleatoriu la viteze mari, nu interacționează între ele și sunt adimensionale. Un astfel de model este foarte simplu în ceea ce privește descrierea sa matematică.
Conform definiției unui proces adiabatic, următoarea expresie poate fi scrisă în conformitate cu prima lege a termodinamicii:
dU=-PdV.
Cu alte cuvinte, un gaz, care se extinde sau se contractă, funcționează PdV datorită unei modificări corespunzătoare a energiei sale interne dU.
În cazul unui gaz ideal, dacă folosim ecuația de stare (legea Clapeyron-Mendeleev), putem obține următoarea expresie:
PVγ=const.
Această egalitate se numește ecuația Poisson. Oamenii care sunt familiarizați cu fizica gazelor vor observa că dacă valoarea lui γ este egală cu 1, atunci ecuația Poisson va intra în legea Boyle-Mariotte (izotermăproces). Cu toate acestea, o astfel de transformare a ecuațiilor este imposibilă, deoarece γ pentru orice tip de gaz ideal este mai mare decât unu. Mărimea γ (gamma) se numește indice adiabatic al unui gaz ideal. Să aruncăm o privire mai atentă asupra semnificației sale fizice.
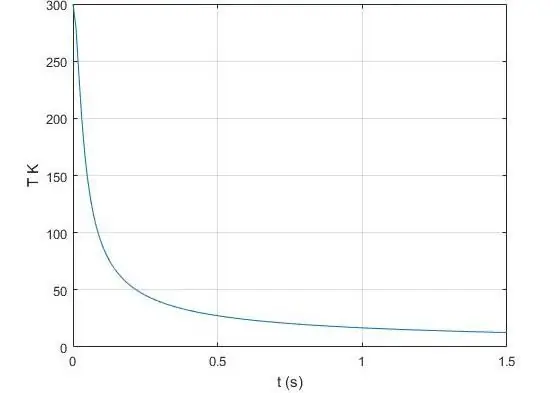
Care este exponentul adiabatic?
Exponentul γ, care apare în ecuația Poisson pentru un gaz ideal, este raportul dintre capacitatea termică la presiune constantă și aceeași valoare, dar deja la volum constant. În fizică, capacitatea de căldură este cantitatea de căldură care trebuie transferată sau preluată dintr-un sistem dat pentru ca acesta să-și schimbe temperatura cu 1 Kelvin. Vom nota capacitatea de căldură izobară cu simbolul CP, iar capacitatea de căldură izobară cu simbolul CV. Atunci egalitatea este valabilă pentru γ:
γ=CP/CV.
Deoarece γ este întotdeauna mai mare decât unu, arată de câte ori capacitatea termică izobară a sistemului de gaz studiat depășește caracteristica izocoră similară.
Capacitățile termice ale CP și CV
Pentru a determina exponentul adiabatic, ar trebui să înțelegem bine semnificația cantităților CP și CV. Pentru a face acest lucru, vom efectua următorul experiment de gândire: imaginați-vă că gazul se află într-un sistem închis într-un vas cu pereți solizi. Dacă vasul este încălzit, atunci toată căldura comunicată va fi convertită în mod ideal în energia internă a gazului. Într-o astfel de situație, egalitatea va fi valabilă:
dU=CVdT.
ValoareCV definește cantitatea de căldură care trebuie transferată sistemului pentru a-l încălzi izocoric cu 1 K.
Acum să presupunem că gazul este într-un vas cu un piston în mișcare. În procesul de încălzire a unui astfel de sistem, pistonul se va mișca, asigurându-se menținerea unei presiuni constante. Deoarece entalpia sistemului în acest caz va fi egală cu produsul dintre capacitatea termică izobară și modificarea temperaturii, prima lege a termodinamicii va lua forma:
CPdT=CVdT + PdV.
De aici se poate observa ca CP>CV, deoarece in cazul unei schimbari izobare de stari este necesar sa se cheltuiește căldură nu numai pentru a crește temperatura sistemului și, prin urmare, energia sa internă, ci și munca efectuată de gaz în timpul expansiunii sale.
Valoarea lui γ pentru un gaz monoatomic ideal
Cel mai simplu sistem de gaz este un gaz ideal monoatomic. Să presupunem că avem 1 mol dintr-un astfel de gaz. Amintiți-vă că în procesul de încălzire izobară a 1 mol de gaz cu doar 1 Kelvin, funcționează egal cu R. Acest simbol este folosit în mod obișnuit pentru a desemna constanta universală a gazului. Este egal cu 8, 314 J / (molK). Aplicând ultima expresie din paragraful anterior pentru acest caz, obținem următoarea egalitate:
CP=CV+ R.
De unde puteți determina valoarea capacității termice izocorice CV:
γ=CP/CV;
CV=R/(γ-1).
Se știe că pentru o alunițăgaz monoatomic, valoarea capacității termice izocorice este:
CV=3/2R.
Din ultimele două egalități urmează valoarea exponentului adiabatic:
3/2R=R/(γ-1)=>
γ=5/3 ≈ 1, 67.
Rețineți că valoarea lui γ depinde numai de proprietățile interne ale gazului însuși (de natura poliatomică a moleculelor sale) și nu depinde de cantitatea de substanță din sistem.
Dependența lui γ de numărul de grade de libertate
Ecuația pentru capacitatea termică izocoră a unui gaz monoatomic a fost scrisă mai sus. Coeficientul 3/2 care a apărut în el este legat de numărul de grade de libertate dintr-un atom. Are capacitatea de a se mișca doar în una dintre cele trei direcții ale spațiului, adică există doar grade de libertate de translație.
Dacă sistemul este format din molecule diatomice, la cele trei de translație se mai adaugă două grade de rotație. Prin urmare, expresia pentru CV devine:
CV=5/2R.
Atunci valoarea lui γ va fi:
γ=7/5=1, 4.
Rețineți că molecula diatomică are de fapt încă un grad de libertate vibrațională, dar la temperaturi de câteva sute de Kelvin nu este activată și nu contribuie la capacitatea de căldură.
Dacă moleculele de gaz constau din mai mult de doi atomi, atunci vor avea 6 grade de libertate. Exponentul adiabatic în acest caz va fi egal cu:
γ=4/3 ≈ 1, 33.
DeciAstfel, pe măsură ce numărul de atomi dintr-o moleculă de gaz crește, valoarea lui γ scade. Dacă construiți un grafic adiabatic în axele P-V, veți observa că curba pentru un gaz monoatomic se va comporta mai brusc decât pentru unul poliatomic.
Exponent adiabatic pentru un amestec de gaze
Am arătat mai sus că valoarea lui γ nu depinde de compoziția chimică a sistemului de gaze. Totuși, depinde de numărul de atomi care alcătuiesc moleculele sale. Să presupunem că sistemul este format din N componente. Fracția atomică a componentului i din amestec este ai. Apoi, pentru a determina exponentul adiabatic al amestecului, puteți folosi următoarea expresie:
γ=∑i=1N(aiγ i).
Unde γi este valoarea γ pentru a-a componentă.
De exemplu, această expresie poate fi folosită pentru a determina γ de aer. Deoarece este format din 99% molecule biatomice de oxigen și azot, indicele său adiabatic ar trebui să fie foarte apropiat de valoarea de 1,4, ceea ce este confirmat de determinarea experimentală a acestei valori.






