Studiarea proprietăților unui gaz ideal este un subiect important în fizică. Introducerea în caracteristicile sistemelor de gaze începe cu luarea în considerare a ecuației Boyle-Mariotte, deoarece este prima lege descoperită experimental a unui gaz ideal. Să o luăm în considerare mai detaliat în articol.
Ce se înțelege prin gaz ideal?
Înainte de a vorbi despre legea Boyle-Mariotte și ecuația care o descrie, să definim un gaz ideal. Este înțeles în mod obișnuit ca o substanță fluidă în care particulele care o alcătuiesc nu interacționează între ele, iar dimensiunile lor sunt neglijabil de mici în comparație cu distanța medie între particule.
De fapt, orice gaz este real, adică atomii și moleculele sale constitutive au o anumită dimensiune și nu interacționează între ele cu ajutorul forțelor van der Waals. Cu toate acestea, la temperaturi absolute ridicate (mai mult de 300 K) și la presiuni scăzute (mai puțin de o atmosferă), energia cinetică a atomilor și moleculelor este mult mai mare decât energia interacțiunilor van der Waals, deci gazul real la valoarea indicată.condițiile cu precizie ridicată pot fi considerate ideale.
Ecuația Boyle-Mariotte
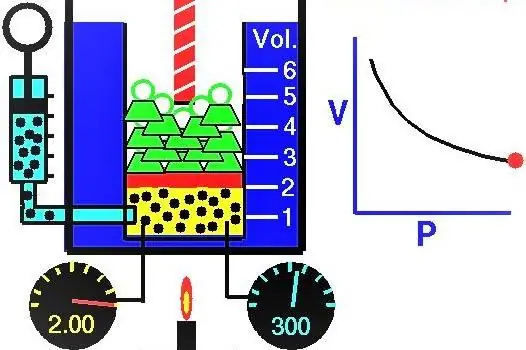
Proprietățile gazelor pe care oamenii de știință europeni le-au explorat activ în secolele XVII-XIX. Prima lege a gazelor care a fost descoperită experimental a fost legea care descrie procesele izoterme de expansiune și comprimare a unui sistem de gaze. Experimentele corespunzătoare au fost efectuate de Robert Boyle în 1662 și Edm Mariotte în 1676. Fiecare dintre acești oameni de știință a arătat în mod independent că în timpul unui proces izoterm într-un sistem de gaz închis, presiunea se modifică invers cu volumul. Expresia matematică obţinută experimental a procesului se scrie sub următoarea formă:
PV=k
Unde P și V sunt presiunea din sistem și volumul acestuia, k este o constantă, a cărei valoare depinde de cantitatea de substanță gazoasă și de temperatura acesteia. Dacă construiți dependența funcției P(V) pe un grafic, atunci va fi o hiperbolă. Un exemplu de aceste curbe este prezentat mai jos.
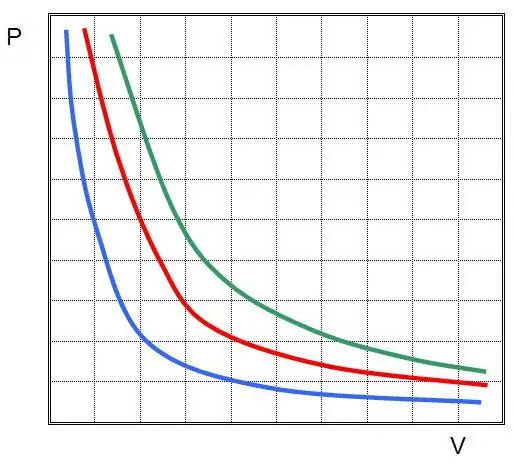
Egalitatea scrisă se numește ecuația Boyle-Mariotte (lege). Această lege poate fi formulată pe scurt după cum urmează: dilatarea unui gaz ideal la o temperatură constantă duce la o scădere proporțională a presiunii în acesta, dimpotrivă, compresia izotermă a unui sistem de gaz este însoțită de o creștere proporțională a presiunii în acesta.
Ecuația gazului ideal
Legea Boyle-Mariotte este un caz special al unei legi mai generale care poartă numele lui Mendeleev șiClapeyron. Emile Clapeyron, rezumând informațiile experimentale despre comportamentul gazelor în diferite condiții externe, în 1834 a obținut următoarea ecuație:
PV=nRT
Cu alte cuvinte, produsul dintre volumul V al unui sistem de gaz și presiunea P din acesta este direct proporțional cu produsul dintre temperatura absolută T și cantitatea de substanță n. Coeficientul acestei proporționalități este notat cu litera R și se numește constanta universală a gazului. În ecuația scrisă, valoarea lui R a apărut datorită înlocuirii unui număr de constante, care a fost făcută de Dmitri Ivanovici Mendeleev în 1874.
Din ecuația universală de stare este ușor de observat că constanța temperaturii și cantitatea de substanță garantează invarianța părții drepte a ecuației, ceea ce înseamnă că și partea stângă a ecuației va rămâne constantă.. În acest caz, obținem ecuația Boyle-Mariotte.

Alte legi privind gazele
Ecuația Clapeyron-Mendeleev scrisă în paragraful de mai sus conține trei parametri termodinamici: P, V și T. Dacă fiecare dintre ei este fix, iar celorlalți doi li se permite să se schimbe, atunci obținem Boyle-Mariotte, Ecuațiile lui Charles și Gay-Lussac. Legea lui Charles vorbește despre o proporționalitate directă între volum și temperatură pentru un proces izobar, iar legea lui Gay-Lussac afirmă că în cazul unei tranziții izocorice, presiunea gazului crește sau scade direct proporțional cu temperatura absolută. Ecuațiile corespunzătoare arată astfel:
V/T=const când P=const;
P/T=const când V=const.
DeciAstfel, legea lui Boyle-Mariotte este una dintre cele trei legi principale ale gazelor. Totuși, diferă de restul în ceea ce privește dependența grafică: funcțiile V(T) și P(T) sunt drepte, funcția P(V) este o hiperbolă.
Exemplu de sarcină pentru aplicarea legii Boyle-Mariotte
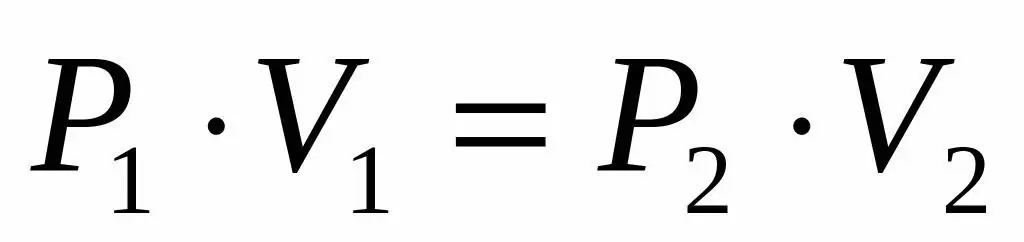
Volumul de gaz din cilindrul de sub piston în poziția inițială a fost de 2 litri, iar presiunea acestuia a fost de 1 atmosferă. Care a fost presiunea gazului după ce pistonul a crescut și volumul sistemului de gaz a crescut cu 0,5 litri. Procesul este considerat izotermic.
Deoarece ni se dau presiunea și volumul unui gaz ideal și știm, de asemenea, că temperatura rămâne neschimbată în timpul expansiunii sale, putem folosi ecuația Boyle-Mariotte sub următoarea formă:
P1V1=P2V 2
Această egalitate spune că produsul volum-presiune este constant pentru fiecare stare a gazului la o anumită temperatură. Exprimând valoarea P2 din egalitate, obținem formula finală:
P2=P1V1/V 2
Când faceți calcule de presiune, puteți utiliza unități din afara sistemului în acest caz, deoarece litrii se vor micșora și obținem presiunea P2 în atmosfere. Înlocuind datele din condiție, ajungem la răspunsul la întrebarea problemei: P2=0,8 atmosfere.






